AbstractPurpose:This study aimed to investigate clinical outcomes of breast cancer patients who underwent mastectomy with or without immediate breast reconstruction.
Methods:Of 1,847 patients undergoing total mastectomy, 371 (20.1%) underwent immediate reconstruction between January 2005 and December 2011. Clinicopathological characteristics and survival were compared by performing univariate and multivariate analysis.
Results:The proportion of reconstruction had been gradually increasing since 2009. Reconstruction group showed younger age at diagnosis and lower cancer stages. Adjuvant chemotherapy and radiation therapy were more frequently administered in the mastectomy alone group. During a median follow-up period of 57 months, locoregional relapse-free survival (LRRFS) was similar regardless of type of surgery. However the reconstruction group showed a more favorable overall survival (OS). Multivariate analysis for LRRFS revealed no statistical significance but the OS was higher in the reconstruction group. In the mastectomy alone group, two-thirds died of breast cancer, while all patients in the reconstruction group died of breast cancer. Stage-matched breast cancer specific survival was similar between both groups.
서 론유방 재건술은 유방암 치료를 위해 유방 절제술을 받은 환자에게 원래의 유방형태로 복원해 주기 위한 수술이다. 우리나라 여성에서 유방암 발병률은 점차 증가하고 있을 뿐만 아니라[1], 한국유방암학회의 보고에 의하면 유방암 발생 연령이 30대가 12.7%, 40대가 37.1%로 젊은 환자에서 많이 발생하고 있다. 이와 함께 유방 검진의 증가와 진단기술의 발달로 유방암의 조기 발견이 늘어나고 있으며, 삶의 질 향상을 위하여 유방 절제술 후 동시 또는 지연 유방 재건술에 대한 수요도 증가하고 있다[2].
유방 재건술은 유방 절제술 후 신체 이미지 손상에 대한 상실감을 줄여주고 환자의 삶의 질을 향상 시켜주는 장점이 있다[3]. 유방 재건술은 시술 시기에 따라 크게 종양제거 수술과 함께 동시에 유방을 복원하는 즉시 재건술과 유방 절제술 후 보조적 치료를 완료한 후 시행하는 지연 재건술 두 가지로 나뉜다. 현재까지 시행되고 있는 대표적인 유방 재건술의 방법은 크게 두 가지로 조직확장기와 보형물을 이용하는 것과 환자 자신의 근육, 지방 그리고 피부를 포함한 자가조직을이용하는피판술이있다.
유방 절제술 후 유방 재건술은 보편화 되고 있지만 재건수술이 가능한 환자를 선택하는 것과 재건수술 시기나 방법을 결정하는 것에 대한 일관된 지침은 미흡한 상태이다. 즉시 재건술에 대한 종양학적인 안정성은 여러 연구들에 의해 밝혀지고 있다[4-8]. Knottenbelt 등[4]은 즉시 재건술 후 국소 재발률과 생존율에 차이가 없으며 국소 재발의 진단을 늦추지 않고 보조 항암요법 치료 결과에도 영향을 미치지 않는다고 보고하였으며, Bezuhly 등[6]은 즉시 재건술 후 유방암 특이 생존율이 젊은 환자에 있어서 증가한다고 보고하였다.
방 법2005년 1월부터 2011년 12월까지 연세대학교 의과대학 세브란스병원에서 원발성 유방암으로 진단받고 유방 전절제술을 시행받은 환자를 대상으로 후향적 연구를 진행하였다. 유방보존술을 받은 환자, 수술 전 항암약물치료를 받은 환자, 전이성 유방암이나 악성 엽상종양 등의 비상피기원 유방암 환자 그리고 지연 재건술을 받은 환자를 제외한 총 1,847명의 환자를 대상으로 하였다. 본 연구는 세브란스병원 연구심의위원회(Institutional Review Board)의 승인 하에 진행하였다(승인번호: 4-2014-0589).
세브란스병원 유방암전문클리닉 등록 자료와 환자의 의무기록 검토를 통하여 환자의 나이, 종양의 크기, 액와 림프절 전이 여부, 유방암 병기, 조직학적 형태와 등급, 호르몬 수용체 발현 유무, 성장인자 수용체 유형 2 (HER2) 과발현 유무, 재발이나 사망 자료를 조사하였다. 미국임상종양학회/미국병리학회(American Society Clinical Oncology/College of American Pathologists) 권고안에 따라 면역조직화학염색법을 이용하여 종양의 핵 내 염색이 1% 이상인 경우 호르몬 수용체 양성으로 정의하였다[11]. HER2의 경우 면역조직화학염색에 의한 점수가 3+이거나, 2+인 경우는 형광동소교잡반응(fluorescence in situ hybridization) 검사상 유전자 증폭이 확인된 경우를 양성으로 정하였다.
생존율은 무국소영역재발 생존율(locoregional relapse-free survival)과 전체 생존율(overall survival)을 비교하였다. 국소영역 재발은 동측 피부나 흉벽에 암이 다시 발생한 경우 또는 동측 액와부, 쇄골상하 림프절이나 내유 림프절에 암이 재발한 경우로 정의하였다. 수술일로부터 사망 원인에 상관없이 사망 유무가 확인되거나 마지막 추적 관찰된 날까지를 전체 생존기간으로 정의하였다.
유방 전절제술을 시행한 군과 유방 전절제술 후 즉시 유방 재건술을 받은 군 간의 임상병리학적 특성이나 보조치료 방법의 비교는 교차분석을 이용하였다. 유방 재건술 유무에 따른 유방암 환자의 국소영역 재발률과 생존율의 차이는 Kaplan-Meier 분석 후 logrank 검정으로 유의성을 평가하였으며, 콕스 비례위험 모형(Cox proportional hazard model)을 이용하여 독립적인 설명변수를 알아보았다. 통계분석은 SPSS version 20.0 (IBM Corp., Armonk, USA) 프로그램을이용하였으며, p값이 0.05 미만인 경우 통계학적으로 유의하다고 판정하였다.
결 과환자의 임상병리학적 특징대상 환자 1,847명의 평균 나이는 51.3±11.0세였으며, 중앙 추적 관찰 기간은 57개월(범위, 1–108개월)이었다. 전체 환자 중 유방 전절제술 후 즉시 유방 재건술을 시행 받은 환자는 371명(20.1%)이었다. 유방 재건 방법으로 조직확장기과 보형물을 이용한 환자는 163명(43.9%)이었으며, 자신의 근육, 지방 그리고 피부를 포함한 자가 조직을 이용하는 피판수술을 받은 환자는 208명(56.1%)이었다. 수술 연도에 따라 즉시 유방 재건술의 비율은 2009년도부터 점차 증가 추세를 보이고 있으며, 2011년도에는 약 1/3의 환자에서 동시 재건술이 시행되었다(Figure 1).
환자의 나이, 종양의 크기, 액와 림프절 상태, 암 병기, 조직학적 형태와 등급, 에스트로겐 및 프로게스테론 수용체, HER2 발현 상태 등은 Table 1과같다. 유방 전절제술만을 시행 받은 환자와 비교하여 즉시 유방 재건술을 시행 받은 경우 40세 이하의 젊은 환자가 약 40%로더많았으며, 종양과 액와 림프절의 병기가 낮아 약 70%의 환자는 암 병기 0–1기였다. 에스트로겐 수용체 발현이나 HER2 상태는 두 군 간에 차이가 없었으나, 폐경 후 여성의 빈도가 높은 유방 전절제술만을 시행 받은 환자 군의 경우 프로게스테론 수용체의 양성 발현 빈도는 즉시 유방 재건술을 시행 받은 환자 군보다 낮았다.
수술 후 보조요법(adjuvant therapy)으로는 방사선치료, 항암약물치료, 항호르몬치료, 표적치료가 시행되었으며, 진행된 암 병기 환자의 비율이 높은 유방 전절제술만을 받은 군에서 방사선치료와 항암약물치료를 받은 환자가 통계학적으로 유의하게 많은 것으로 나타났다(Table 1).
수술 방법에 따른 생존율 분석추적 기간 동안 국소영역 재발은 대상 환자 1,847명 중 48예(2.6%)에서 발생하였다. 유방 전절제술 시행 군에서 42예(2.8%), 즉시 재건술 환자에서 6예(1.6%) 확인되었다. Kaplan-Meier 방법을 이용한 생존율 비교에서 즉시 유방 재건술의 시행 여부에 상관없이 무국소영역재발 생존율은 통계학적으로 유의한 차이가 없었다(Figure 2A). 유방 전절제술을 시행 받은 군의 5년 무국소영역재발 생존율은 96.7%였으며, 즉시 재건술을 시행 받은 군의 5년 무국소영역재발 생존율은 98.1%였다.
하지만 전체 생존율 분석에서는 통계적으로 유의하게 유방 전절제술만 시행 받은 환자 군의 예후가 불량하였다(Figure 2B). 유방 전절제술을 시행 받은 군의 5년 전체 생존율은 92.7%였으며, 즉시 재건술을 시행 받은 군의 5년 전체 생존율은 98.8%였다(p < 0.001). 즉시 유방 재건술을 받은 환자만을 대상으로 보형물을 이용한 재건술과 자가 조직을 이용한 재건술 사이의 무국소영역재발 생존율이나 전체 생존율은 유방 재건술의 방법에 따라 통계적인 차이는 발견되지 않았다.
생존율의 다변량 분석과 사망 원인다른 임상병리학적 특성과 수술 후 보조치료 요법을 보정한 다변량 분석에서도 즉시 유방 재건술 여부에 따라 무국소영역재발 생존율은 통계학적인 유의성을 보이지 않았다. 종양의 크기와 림프절 전이 유무가 국소영역 재발과 관련된 독립적인 예후인자였다(Table 2). 하지만 전체 생존율을 다변량 분석한 결과 즉시 유방 재건술을 시행 받은 경우 위험비가 0.182 (95% 신뢰구간, 0.06–0.50)로 통계적으로 유의하게 생존율이 양호하였다(Table 2). 종양의 크기가 큰 경우나 액와 림프절 전이가 있는 경우는 불량한 전체 생존율을 보이는 예후인자였으며, 항암약물치료와 항호르몬치료를 시행한 경우는 양호한 전체 생존율의 독립적인 예후인자였다.
암 병기를 일치시켜 무국소영역재발 생존율을 비교하였을 때 암 병기 0–1기, 2기와 3기 각각에서 유방 재건술의 여부에 상관없이 통계적으로 차이가 없었다(Figure 3). 암 병기를 일치시킨 전체 생존율 분석에서는 암병기 0–1기인 경우 즉시 유방 재건술을 받은 군이 통계적으로 양호한 생존을 보였다(Figure 4A). 암 병기 2기와 3기에서는 유방 전절제술만 받은 군의 생존이 불량한 경향성을 보였으나 통계적인 유의성은 없었다(Figure 4B, C).
추적 기간 동안 총 103명(5.6%)의 환자가 사망하였으며, 사망 원인이 확인되지 않은 7명을 제외하고, 유방 재건술을 받은 환자 중 4명이 사망하였으며, 재건술에 의한 합병증과 관련된 사망은 없었고 모두 유방암으로 사망하였다. 유방 전절제술만 받은 환자 중 사망 원인이 확인된 92명중 34명(37.0%)은 유방암 이외의 원인으로 사망하였으며, 58명(63.0%)은 유방암으로 사망하였다. 암 병기를 일치시킨 후 유방암 특이 생존율을 확인하였을 때, 유방 재건술의 유무에 상관없이 유방암 특이 생존율은 통계적으로 차이가 없었다.
고 찰유방암은 세계 전체 여성 암의 23%를 차지하며 여성 암 중 최다 발생률을 보인다. 우리나라에서는 갑상선암에 이어 두 번째로 흔한 암으로 점차 발생이 증가하고 있다[1]. 유방암에 대한 여성들의 관심과 유방 검진의 증가에 따라 초기 유방암으로 진단되는 환자들과 젊은 유방암 환자들의 발생 빈도가 점차 증가하는 추세이며, 이와 더불어 삶의 질 향상을 위해 유방 재건술을 받는 경우도 해마다 증가하고 있다[2]. 한국유방암학회의 보고에 의하면[12], 2000년보다 2011년에는 유방 재건수술이 7배 이상 증가했으며 본 연구에서도 2009년부터 점차 증가하는 추세를 보이고 있다(Figure 1).
유방 재건술은 보형물을 이용한 재건 방법과 자가조직을 이용한 방법으로나뉘어진다. 보형물을 이용한 유방 재건술은 수술이 간단하고, 추가적인 흉터가 생기지 않으며, 비용이 저렴하고, 회복 기간이 빠르다는 장점이 있으나, 이물질에 대한 거부감, 감염, 피막구축 등의 합병증, 보형물의 내구성 및 수명 등의 단점이 있다[13]. 자가조직을 이용한 재건 시에는 이와 같은 합병증은 없거나 드물지만, 피판의 괴사, 긴 수술시간 및 회복기간 그리고 공유부에 생기는 후유증의 문제가 있다[14]. 양자 간에는 차이가 있지만 즉시 유방 재건술은 유방 절제술 후 신체의 손상에 대한 두려움과 정신적인 고통을 피할수있으며 유방 절제술과 유방재건술을 동시에 실시함으로써 수술의 횟수도 줄일 수 있는 장점이 있다.
유방암 절제술 후 유방 재건술이 점차 보편화 되고 있지만 재건수술이 가능한 환자를 선택하는 것과 재건수술 시기나 방법을 결정하는 것에 대한 일관된 지침은 미흡한 상태이다. 유방 재건술 후 국소영역 재발의 발견과 치료에 방해를 받지 않을까 하는 염려, 국소영역 재발의 증가, 수술 후 보조치료 계획에 영향을 주지 않을까 하는 걱정, 그리고 이에 따르는 생존율에 미치는 영향을 고려해야 한다는 의견들도 있다[9,10,15]. 또한 Isern 등[16]은 지연 재건술을 받은 환자들에서 국소영역 재발률이 2.08배 높다고 보고하기도 하였다. 이와는 달리 Knottenbelt 등[4]은 즉시 재건술 후 5년 무병생존율(disease-free survival) 93%로 생존율에 차이가 없으며 국소 재발의 진단을 늦추지 않고 보조 항암요법치료 결과에도 영향을 미치지 않는다고 보고하였으며, Bezuhly 등[6]은 즉시 재건술 후 유방암 특이 생존율이 재건술을 받지 않은 군에 비해 증가한다고 보고하였으며(위험비, 0.74; 95% 신뢰구간, 0.68–0.80), 특히 50세 미만의 환자에 있어서 증가한다고 보고하였다(위험비, 0.47; 95% 신뢰구간, 0.28–0.80). 본 연구에서도 즉시 유방 재건술을 받은 환자에서 국소영역 재발률은 유방 절제술만을 받은 환자와 차이가 없었다.
하지만 전체 생존율을 단변량 분석하였을 때 즉시 유방 재건수술을 시행 받은 환자군의 생존율이 더 높았다. 이는 본 연구가 후향적 분석으로 조사하였기 때문에 환자군의 선택 편향과 연관된 것으로 사료된다. 대상 환자들의 임상병리학적 특성을 비교하였을 때 즉시 유방 재건술을 받은 환자에서 평균 진단 시 연령이 낮고 암 병기가 낮았다. 즉시 유방 재건술을 받은 환자 중 40대 이하는 39.6%로 유방 절제술만을 받은 군의 11.5%에 비해 높았으며, TNM 병기에서도 암 병기 0–1은 즉시 유방 재건술을 받은 환자에서 68.5%로 유방 전절제술만 받은 군의 50.6%에 비해 높은 비율을 차지하고 있었다. 원발종양이 큰 경우와 액와 임파선 전이가 있는 경우 국소 재발이나 원격 전이의 확률이 높음은 잘 알려져 있으며 이러한 차이가 생존율에 영향을 미칠 수 있을 것으로 생각된다.
본 연구의 대상 환자군의 임상병리학적 특성이 달랐으므로 선택 편향을 보정하기 위하여 다변량 분석을 시행한 결과 수술 방법에 따라 무국소영역재발 생존율은 통계적 유의성이 없었다. 하지만 유방 절제술만 시행한 군의 전체 생존율은 즉시 재건술을 시행한 경우보다더 불량하였다. 이는 상대적으로 고령의 환자가 유방 절제술만 시행한 군에 더 많았으며, 사망 원인 조사에서 유방 절제술만 시행한 군의 사망 환자 중 1/3은 유방암 이외의 원인으로 사망한 것으로 보아 유방암 재발 이외의 원인이 연관된 것으로 생각된다. 이를 확인하기 위해 병기를 일치시킨 후 유방암 특이 생존율을 분석한 결과 두 군 간에 통계적 유의성은 확인할 수 없었다. 이러한 결과는 즉시 유방 재건술의 종양학적 안정성을 보여주는 결과라 할 수 있으며 이는 다른 연구 결과와 동일하다[4-8].
본 연구의 제한점은 먼저 중앙 추적관찰 기간이 57개월로 생존율을 평가하기에는 짧은 기간이라는 것이다. 추적 기간 중 사망은 5.6%에서만 발생하였으므로 생존율의 해석에 주의가 필요하다. 향후 추적 관찰 기간이 늘어난다면 결과가 달라질 가능성이 있으므로 장기간 추적 관찰 연구가 필요할 것으로 사료된다. 또한 재건술 후 보조치료의 지연 여부와 예후와의 상관성에 논란이 있었으나 본 연구에서는 보조치료의 방법에 따른 시작 시기, 종류나 횟수 등에 관해 분석이 되지 않아 추가 연구가 필요할 것으로 생각된다.
본 연구에서는 유방암으로 유방 절제수술과 동시에 재건수술을 받은환자와 재건술을 시행하지 않은 환자의 임상적 결과 비교를 통해 두 군 간에 국소 재발률이나 치료 성적에 차이가 없음을 확인하였다. 유방암 환자의 유방 절제술 후 즉시 재건술은 적절한 복원 방법과 술기의 적용으로 비교적 안전하게 시행될 수 있다. 유방암환자의 안전한 종양 치료와 완전한 일상 생활이나 사회 생활의 복귀를 위해서 수술 전 즉시 재건술에 대한 외과와 성형외과뿐만 아니라 종양내과, 방사선종양학과 등 유방암 다학제 진료 팀에 의한 상담과 치료 계획 수립은 유방암 환자들의 삶의 질 향상에 기여할 것으로 생각된다.
Figure 2.Survival of patients undergoing mastectomy with or without immediate reconstruction. (A) Locoregional relapse-free survival was similar regardless of type of surgery. (B) Overall survival was favorable in the reconstruction group. 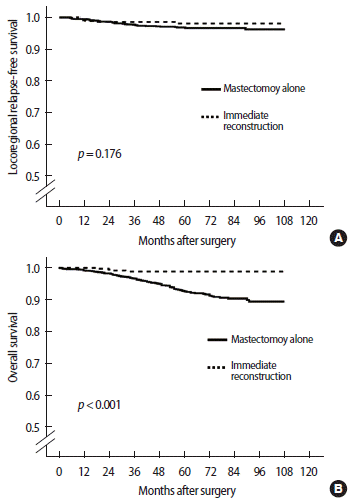
Figure 3.Stage-matched locoregional relapse-free survival curve. (A) Stage 0–1. (B) Stage 2. (C) Stage 3. 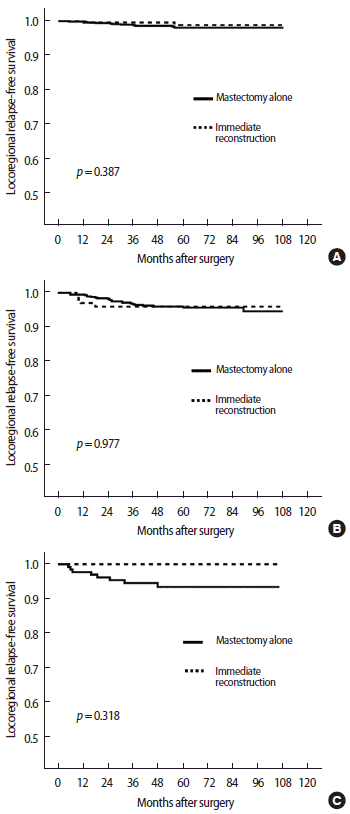
Table 1.Clinicopathologic characteristics and adjuvant therapies of patients undergoing mastectomy with or without immediate reconstruction Table 2.Cox proportional hazards model for survival REFERENCES1. Park SK, Kang D, Kim Y, Yoo KY. Epidemiologic characteristics of the breast cancer in Korea. J Korean Med Assoc 2009;52:937-45.
2. Enewold LR, McGlynn KA, Zahm SH, Poudrier J, Anderson WF, Shriver CD, et al. Breast reconstruction after mastectomy among Department of Defense beneficiaries by race. Cancer 2014;120:3033-9.
3. Guyomard V, Leinster S, Wilkinson M. Systematic review of studies of patients’ satisfaction with breast reconstruction after mastectomy. Breast 2007;16:547-67.
4. Knottenbelt A, Spauwen PH, Wobbes T. The oncological implications of immediate breast reconstruction. Eur J Surg Oncol 2004;30:829-33.
5. Sandelin K, Wickman M, Billgren AM. Oncological outcome after immediate breast reconstruction for invasive breast cancer: a longterm study. Breast 2004;13:210-8.
6. Bezuhly M, Temple C, Sigurdson LJ, Davis RB, Flowerdew G, Cook EF Jr. Immediate postmastectomy reconstruction is associated with improved breast cancer-specific survival: evidence and new challenges from the Surveillance, Epidemiology, and End Results database. Cancer 2009;115:4648-54.
7. Le GM, O’Malley CD, Glaser SL, Lynch CF, Stanford JL, Keegan TH, et al. Breast implants following mastectomy in women with early-stage breast cancer: prevalence and impact on survival. Breast Cancer Res 2005;7:R184-93.
8. Baker JL, Mailey B, Tokin CA, Blair SL, Wallace AM. Postmastectomy reconstruction is associated with improved survival in patients with invasive breast cancer: a single-institution study. Am Surg 2013;79:977-81.
9. Alderman AK, Hawley ST, Waljee J, Mujahid M, Morrow M, Katz SJ. Understanding the impact of breast reconstruction on the surgical decision-making process for breast cancer. Cancer 2008;112:489-94.
10. Alderman AK, Hawley ST, Waljee J, Morrow M, Katz SJ. Correlates of referral practices of general surgeons to plastic surgeons for mastectomy reconstruction. Cancer 2007;109:1715-20.
11. Rakha EA, Starczynski J, Lee AH, Ellis IO. The updated ASCO/CAP guideline recommendations for HER2 testing in the management of invasive breast cancer: a critical review of their implications for routine practice. Histopathology 2014;64:609-15.
12. Kim Z, Min SY, Yoon CS, Lee HJ, Lee JS, Youn HJ, et al. The basic facts of korean breast cancer in 2011: results of a nationwide survey and breast cancer registry database. J Breast Cancer 2014;17:99-106.
13. Cordeiro PG, McCarthy CM. A single surgeon’s 12-year experience with tissue expander/implant breast reconstruction: part II. An analysis of long-term complications, aesthetic outcomes, and patient satisfaction. Plast Reconstr Surg 2006;118:832-9.
14. Kim EK, Eom JS, Ahn SH, Son BH, Lee TJ. Evolution of the pedicled TRAM flap: a prospective study of 500 consecutive cases by a single surgeon in Asian patients. Ann Plast Surg 2009;63:378-82.
|
|
||||||||||||||||||||||||||||||||